國(guó)際頂級(jí)期刊《自然》旗下《信號(hào)轉(zhuǎn)導(dǎo)與靶向治療》雜志�����,近日發(fā)表了一篇題為“中國(guó)創(chuàng)新藥發(fā)展和監(jiān)管支持的現(xiàn)狀”的綜述文章�,系統(tǒng)回顧了中國(guó)創(chuàng)新藥的跨越式發(fā)展歷程,以及中國(guó)藥品審評(píng)審批制度改革帶來(lái)的變化�。文章選用了部分中國(guó)研發(fā)新藥案例,而首個(gè)被頂刊點(diǎn)名的"中國(guó)新藥樣本"�,是一款治療皮膚病、名為本維莫德的1類新藥,成為了中國(guó)藥審改革最硬的“新藥勛章”�����。

文章數(shù)據(jù)顯示�,2019-2023年間,中國(guó)創(chuàng)新藥研發(fā)實(shí)現(xiàn)跨越式發(fā)展�����。得益于一系列監(jiān)管制度改革�����,新藥臨床試驗(yàn)(IND)與上市申請(qǐng)(NDA)的數(shù)量和批準(zhǔn)率均顯著增長(zhǎng)�,研發(fā)上市周期也明顯縮短�����。同時(shí)�����,研發(fā)管線質(zhì)量持續(xù)提升�����,全球首創(chuàng)First-in-class等高價(jià)值創(chuàng)新藥物增速已超越“Me-too”類,使中國(guó)成為全球第二大創(chuàng)新藥研發(fā)管線持有國(guó)�。中國(guó)深度參與全球多中心臨床試驗(yàn),創(chuàng)新藥出海授權(quán)交易激增�,國(guó)際認(rèn)可度和影響力也快速提升。
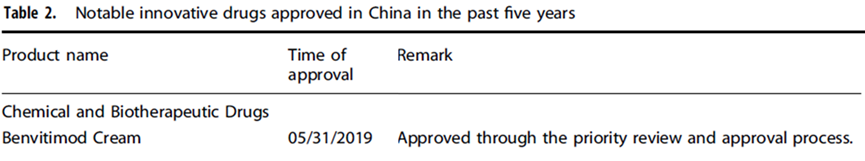
作為擁有自主知識(shí)產(chǎn)權(quán)的全球首創(chuàng)藥物�,本維莫德于2019年率先獲得國(guó)家藥監(jiān)局批準(zhǔn),比美國(guó)FDA早了整整三年�����?����!氨揪S莫德的價(jià)值不僅在于填補(bǔ)了治療領(lǐng)域空白�����,更在于驗(yàn)證中國(guó)藥物監(jiān)管體系的效率和成熟度�����。"清華大學(xué)醫(yī)學(xué)院首席研究員孔繁圃表示�����。
孔繁圃進(jìn)一步解讀表示,首先�,本維莫德乳膏作為中國(guó)原創(chuàng)1類新藥,因其創(chuàng)新結(jié)構(gòu)和臨床價(jià)值�����,獲得國(guó)家藥監(jiān)局(NMPA)優(yōu)先審評(píng)資格�����,實(shí)現(xiàn)了高效審批�����,彰顯中國(guó)監(jiān)管路徑的有效性�。其次�,本維莫德在中國(guó)首發(fā)獲批后,短短三年內(nèi)再獲美國(guó)FDA批準(zhǔn)�����,這一里程碑不僅證明該藥的臨床價(jià)值�����,更標(biāo)志著國(guó)際權(quán)威機(jī)構(gòu)對(duì)中國(guó)創(chuàng)新藥的認(rèn)可。再次�,NMPA對(duì)本維莫德的快速審評(píng),展現(xiàn)了其對(duì)前沿作用機(jī)制(如靶向AhR通路)的科學(xué)判斷力和審評(píng)能力�,這一成功案例推動(dòng)中國(guó)從“仿制藥大國(guó)”向“創(chuàng)新藥策源地”轉(zhuǎn)型,是全球醫(yī)藥領(lǐng)域獲得更高話語(yǔ)權(quán)的標(biāo)志�����。
“過(guò)去是中國(guó)人等西方新藥�����,現(xiàn)在是世界等中國(guó)新藥�����?!北揪S莫德發(fā)明人、上海澤德曼醫(yī)藥科技有限公司董事長(zhǎng)陳庚輝博士指出�,“這種轉(zhuǎn)變背后是我國(guó)藥品監(jiān)管體系的系統(tǒng)性重構(gòu)和進(jìn)步,而這種重構(gòu)在本維莫德升級(jí)產(chǎn)品——澤立美乳膏上得到再一次彰顯�。2024年11月,全球首創(chuàng)無(wú)激素兒童濕疹A(yù)hR新藥澤立美在中國(guó)獲批上市�����,20天之后又獲得FDA批準(zhǔn),獲批速度再一次領(lǐng)先美國(guó)�。本維莫德從科研實(shí)力和獲批速度可謂在國(guó)際上打出了‘雙響炮’!”
分析人士指出�����,依靠制度創(chuàng)新�、市場(chǎng)需求和科研突破的共振,使得澤立美(本維莫德)所代表的“中國(guó)原創(chuàng)�、全球共享”模式正在形成示范效應(yīng)。據(jù)不完全統(tǒng)計(jì)�,2024年我國(guó)創(chuàng)新藥出海總數(shù)達(dá)98筆�,總交易金額攀升至595.505億美元,中國(guó)正在從全球醫(yī)藥創(chuàng)新的追隨者轉(zhuǎn)變?yōu)橹匾暙I(xiàn)和領(lǐng)跑者�����。
這種創(chuàng)新優(yōu)勢(shì)正在轉(zhuǎn)化為患者實(shí)惠�?����?追逼员硎荆瑒?chuàng)新藥不是遙不可及的科技�����,而是能讓老百姓真正用上的治療選擇�。未來(lái),隨著中國(guó)創(chuàng)新藥研發(fā)持續(xù)發(fā)力�,更多“首創(chuàng)新藥”不僅能先在中國(guó)上市,還有望走向全球�����,讓世界見證“中國(guó)好藥”的實(shí)力�����。